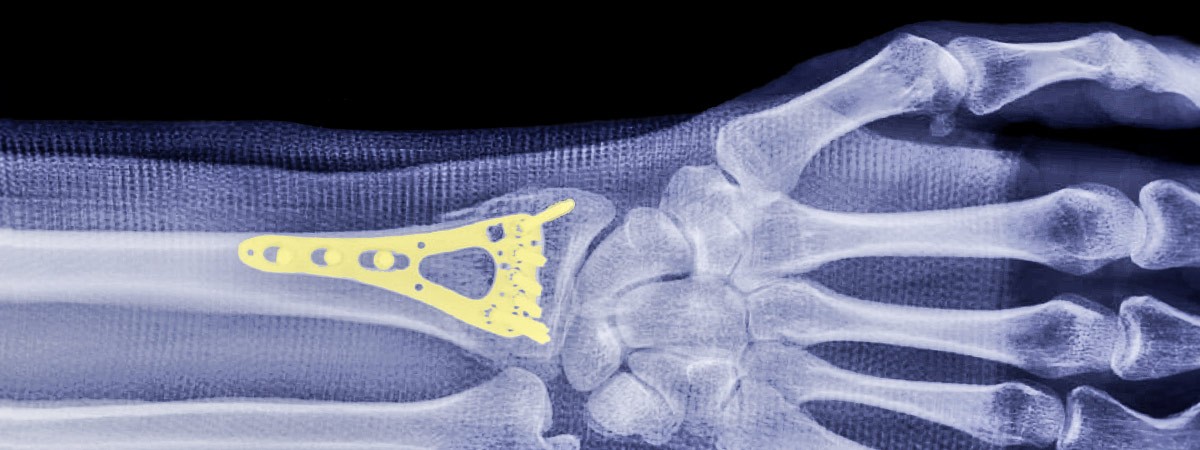
Nowe stawy prosto z drukarki
Dostosowane do wymagań w próżni
W technologii 3D można drukować nie tylko małe elementy z tworzywa sztucznego. Dzięki postępom w produkcji addytywnej z różnych surowców można tworzyć różne kształty. Obecnie metodą druku 3D wytwarza się dopasowane do potrzeb pacjenta implanty ortopedyczne. Pomaga w tym pompa próżniowa od grupy Busch.
Dawniej pacjent oczekujący na implant medyczny miał dwie opcje: standardowy element z katalogu lub bardzo długie oczekiwanie na indywidualne rozwiązanie. Drukowanie 3D umożliwia połączenie najlepszych cech tych opcji: anatomicznie dokładny implant i krótki czas do operacji. Lepsze dopasowanie oznacza również mniejszy dyskomfort podczas rekonwalescencji i mniejsze prawdopodobieństwo konieczności przeprowadzania kolejnych operacji.
Drukowany implant
Każde ciało jest inne. Dlatego tworzenie implantu przy użyciu tradycyjnych technik obróbki metalu może zająć tygodnie żmudnego kształtowania, frezowania i szlifowania w celu uzyskania skomplikowanej formy anatomicznej. Może to także wymagać zastosowania wielu części. Dzięki drukowi 3D proces ten jest mniej pracochłonny. Implant jest mapowany w programie projektowym dzielącym go na setki, a nawet tysiące małych fragmetów. Drukarka 3D „drukuje” następnie wszystkie poszczególne fragmenty, jeden na drugim. Proces, w którym tworzony jest tylko jeden fragment może zostać zakończony w ciągu kilku dni.Skoncentrowane pod próżnią
Metalowe implanty są wytwarzane metodą topienia wiązką elektronów (EBM) w próżni. Najpierw pompa próżniowa firmy Busch usuwa całe powietrze z komory produkcyjnej. Następnie wolframowy drut jest podgrzewany do temperatury 2500°C, co powoduje emisję elektronów. Są one skoncentrowane we wiązce i rzutowane na złoże sproszkowanego metalu, zwykle tytanu lub kobaltu i chromu. Wiązka elektronów podgrzewa i topi cząstki proszku, z którymi styka się, przemierzając kształt określony przez program projektu. W ten sposób na dnie zbiornika proszku powstaje cienka warstwa metalu – dolna warstwa obiektu 3D. Następnie zbiornik jest opuszczany wraz z nadrukowanym materiałem, dodawana jest kolejna porcja proszku, a następna warstwa jest stapiana na pierwszej. Proces ten jest powtarzany aż do ukończenia warstwy końcowej implantu. Proces EBM jest prowadzony pod próżnią z trzech różnych powodów. Pierwszym jest precyzja. W obecności innych cząsteczek gazu wiązka elektronów może z nimi kolidować i odbijać się, powodując niewłaściwe topienie się cząsteczek metalu. Może to wywierać duży wpływ na dokładność produktu końcowego. Próżnia zapewnia również jednorodność materiału: ponieważ w komorze nie ma powietrza, w stopionym metalu nie mogą tworzyć się pęcherzyki. Wreszcie dzięki brakowi tlenu metal nie utlenia się po podgrzaniu. Oznacza to, że pozostałości proszku można wykorzystać ponownie do następnego procesu drukowania.
Przeszczep bez dawcy
Drukowanie z żywymi komórkami brzmi jak film science fiction, ale biodrukowanie tkanki ludzkiej stanowi kolejny krok postępu medycyny. Dzięki zastosowaniu „bioatramentu”, kombinacji ludzkich komórek i różnych biokompatybilnych materiałów, można drukować tkankowe struktury 3D. Mogą to być stosunkowo proste tkanki, takie jak skóra, lub struktury bardziej złożone, takie jak narządy wewnętrzne. Rozwój ten umożliwiłby wykonanie przeszczepów narządów z tkanki własnej odbiorcy – bez konieczności korzystania z dawcy i bez ryzyka odrzucenia. Miałoby to również zastosowanie w testowaniu leków i modelowaniu chorób. Jest to złożony proces, w którym konieczne jest uwzględnienie pewnych aspeków etycznych, ale wykazuje potencjał zrewolucjonizowania opieki zdrowotnej w przyszłości.
Drukowanie z żywymi komórkami brzmi jak film science fiction, ale biodrukowanie tkanki ludzkiej stanowi kolejny krok postępu medycyny. Dzięki zastosowaniu „bioatramentu”, kombinacji ludzkich komórek i różnych biokompatybilnych materiałów, można drukować tkankowe struktury 3D. Mogą to być stosunkowo proste tkanki, takie jak skóra, lub struktury bardziej złożone, takie jak narządy wewnętrzne. Rozwój ten umożliwiłby wykonanie przeszczepów narządów z tkanki własnej odbiorcy – bez konieczności korzystania z dawcy i bez ryzyka odrzucenia. Miałoby to również zastosowanie w testowaniu leków i modelowaniu chorób. Jest to złożony proces, w którym konieczne jest uwzględnienie pewnych aspeków etycznych, ale wykazuje potencjał zrewolucjonizowania opieki zdrowotnej w przyszłości.